来源:奇点网
20多年前,法国科学家Catherine Boileau开启了一个课题:寻找“家族性高胆固醇血症”(Familial Hypercholesterolemia,FH)的致病基因。
顾名思义,FH患者的胆固醇水平比正常人高得多,尤其是“坏胆固醇”——低密度脂蛋白胆固醇(LDL-C)会显著升高。胆固醇高,就可以堆积在全身各处导致症状,比如特征性的手部黄色瘤。
FH患者的另外一大特征,是心血管疾病的发病很早,如果是纯合子型突变的患者,不到三十岁就可能死于冠心病和中风,这可太吓人了。幸好这种情况的发生率很低,属于典型的罕见病[1]。
但杂合子型的FH,在人群中的患病率可就高得多了,大概每200人当中就有一个[1],他们心血管疾病的风险也会明显升高。从基因层面解谜FH,科学家们绝对不缺来源,更不缺动力,谁不想让要命的心血管疾病离自己远一点呢?
不过在解谜FH的路上,科学家们却收获了意外之喜——降脂新药PCSK9抑制剂。最近,PCSK9抑制剂阿利西尤单抗(Alirocumab)就在中国正式获批,而且适应症还一下子批了两个。
除了用于原发性高胆固醇血症(包括杂合子型家族性和非家族性)和混合性血脂异常患者降低LDL-C,这个阿利西尤单抗,还能用于动脉粥样硬化性心血管疾病患者的心血管事件预防,也就是说,它成为了治疗冠心病患者的重量级新药。

注意啊,这个用法属于二级预防(图片来源:Pixabay)
从罕见病的致病靶点,到重磅炸弹级降脂新药,PCSK9是怎么实现华丽转身的?
三个国家,三支团队,三年解谜
PCSK9的解谜之旅,还是要说回FH这种疾病。当时科学界已经发现了两个与FH有关的基因,一个编码大名鼎鼎的载脂蛋白E(APOE),另一个则编码肝细胞表面,与LDL-C的清除关系密切的低密度脂蛋白受体(LDLR)。
但有一些被记录在案的患者家庭,却不存在APOE和LDLR基因的异常。身为遗传学家,Boileau要找的目标,就是这两个基因之外的嫌疑犯。
1999年,Boileau的团队对法国13个FH患者家庭做了基因测序,认为在人体1号染色体短臂上的一个区域,可能藏着导致FH的“第三个致病基因”[2]。
但Boileau和学生们足足分析了50多个基因,都没能找到答案,她本以为还要继续大海捞针,一个个基因分析下去,但在2003年的一天,她的电话响了。这一通电话,让科学史上多了一个“天赐的治疗靶点”。
打电话给Boileau的,是一个同样说法语的科学家。2003年初,加拿大蒙特利尔临床研究所Nabil Seidah的团队,发现了一种“谜一样的蛋白”。

基因层面的事,有时候是挺迷的(图片来源:Pixabay)
说它谜,是因为这个蛋白存在于胚胎发育阶段的大脑神经元、肠道和肝肾等全身多处,但具体作用一时还弄不清[3],于是Seidah把这个蛋白命名为NARC-1(neural apoptosis-regulated convertase 1)。
Seidah想到联系Boileau,是因为NARC-1的编码基因位点,就在1999年Boileau提到的那个1号染色体区域中,而Seidah恰好看过论文,会不会NARC-1就对上了呢?
两位科学家在电话里的对话,实在太有趣了。Seidah的开场白是:“我知道你不认识我,我也不认识你,但我们也许在研究非常相似的东西。”
“你怎么知道你发现的基因,和我要找的基因相同呢?”“我也不确定,但我知道这个基因在肝脏的表达水平很高。”“你疯了。”“那我们打个赌吧,赌一瓶香槟我说得对?”两个星期后,Boileau回了电话:“我欠你三瓶香槟。”
两支研究团队通力合作的成果,发表在了2003年6月的《自然·遗传学》上:大约12.5%的FH患者家庭,存在NARC-1基因的突变,它真的是Boileau要找的“第三个致病基因”[4]。
按照标准命名法,NARC-1换了个正式名字——前蛋白转化酶枯草溶菌素9,也就是PCSK9。动物实验进一步印证了Boileau和Seidah的发现,他们在法国FH患者身上找到的两种PCSK9突变,确实可以使LDLR的水平下降[5]。

但是解开谜题也是很有成就感的(图片来源:Pixabay)
与此同时,两支美国科研团队分别独立证实,PCSK9对LDL-C水平的影响路径,还不只有影响LDLR这一条。准确的说,PCSK9简直就是个猪队友啊。
人体对LDL-C的代谢主要是由肝脏进行。肝细胞表面有可以识别LDL-C的受体LDLR,LDLR识别并结合LDL-C,然后肝细胞把它们一起内吞,降解掉LDL-C,而LDLR却能回到细胞表面,循环利用成百上千次,相当绿色环保。
但有了PCSK9,情况就不同了,它也能结合LDLR,结合后同样也是被肝细胞内吞,但被降解的却不是PCSK9,而是LDLR,清道夫反倒成了被清除的对象。另外,PCSK9还能干扰LDLR回到肝细胞表面的过程,影响LDLR的循环利用[6]。
LDLR被这样前后夹击,肝细胞代谢LDL-C的效率就会大打折扣,结果LDL-C就在体内越堆越多,而当时LDL-C“坏胆固醇”的身份已经是实锤了。
LDL-C越堆越多,心血管疾病的风险就越来越高,降脂的重要性毋庸置疑。从这个角度来说,不对PCSK9下狠手都不行。
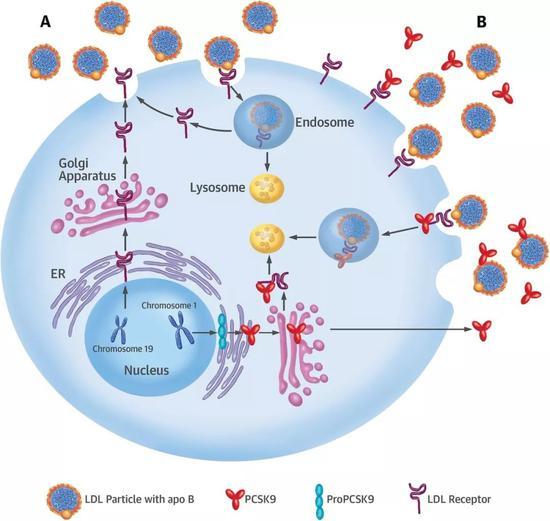
文字描述不够清楚的话,这张图还可以补充说明(图片来源:JACC)
不过,人体内的同一个基因可能有很多种突变方式,Boileau和Seidah找到的是让PCSK9水平升高的突变。假如PCSK9基因发生了功能缺失突变,导致PCSK9在体内水平降低甚至消失,结果会怎么样?
最终回答这个问题的,是美国心脏病学家Helen Hobbs,她在2000年启动了达拉斯心脏研究(Dallas Heart Study),带领团队收集了3500多名受试者的血脂、血压等检测结果,并且对受试者进行了基因测序。
在Hobbs看来,假如受试者的某项检测结果很不寻常,就肯定在基因层面存在相应的罕见变异,这些变异,就提示了可能参与心血管疾病的基因。通过这样的方法挑基因做分析,比直接一个一个基因去验证更简单。
达拉斯心脏研究的初步资料收集完成不久,Boileau和Seidah就发布了他们的科研成果。这让Hobbs很快想到,她收集到的受试者资料中,有些人的LDL-C特别高,有些就特别低,会不会就和特定的PCSK9突变有关?
重做一遍PCSK9基因的测序,Hobbs很快得到了答案:在达拉斯心脏研究入组的近一半黑人当中,大约有2%的人携带了PCSK9功能缺失性突变,这些人的LDL-C水平比不携带突变的人低40%。
40%的下降是什么概念呢?他汀类药物单独使用时需要大剂量甚至是强化剂量,才能让LDL-C下降到这个程度,而且很多患者由于种种原因,还达不到疗效[7]!
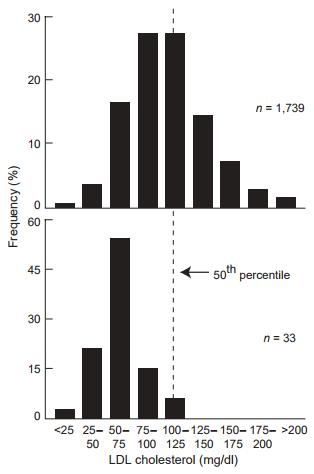
上下两张图是携带/不携带PCSK9基因突变人群,LDL-C水平的对比,中位数差距就说明了整体差异(图片来源:Nature Genetics)
不过,达拉斯心脏研究当时的随访时间还不够,并不能体现PCSK9突变对心血管疾病风险的影响。于是Hobbs又和其他科学家合作,对随访近20年的社区动脉粥样硬化风险研究(ARIC)受试者开展了基因测序和综合分析。
2006年发表在《新英格兰医学杂志》上的测序和分析结果,震惊了整个心血管圈子:ARIC研究的3000多名黑人受试者中,有2.6%携带了PCSK9功能缺失性突变,他们的LDL-C水平比不携带突变的人低28%,冠心病风险则低了88%!
而另外9000多名白人受试者,也有3.2%携带了PCSK9功能缺失性突变,这些人的LDL-C水平比不携带突变的人低了15%,冠心病风险低了47%。达拉斯心脏研究中,Hobbs并没能在白人受试者中测到PCSK9突变,这就填补了空白[8]。
从Boileau的初步探索,到Seidah的关键援手,再到Hobbs提供的实锤,三个国家,三支团队,用三年的时间,神速地完成了PCSK9、LDL-C水平和心血管疾病风险的一整个拼图。

这就是三国情缘啊(图片来源:Pixabay)
但三位科学家中,名气最大的还是Hobbs,因为真正让PCSK9抑制剂的研发狂潮开启的,还是来自她在达拉斯一份意想不到的收获。
敲开降脂难关的“基因敲除人”
开发一种药物,并不是有了靶点就行,各方面的问题都得权衡。就拿PCSK9抑制剂的搭档——兢兢业业的劳模他汀类药物来说,它们的使用就有些老毛病。
奇点糕之前也提过,使用他汀类药物,在当时虽然能把心血管疾病患者的LDL-C水平降低大约三分之一,但是患者需要长期服药,这就肯定有依从性上的问题,毕竟坚持吃药不容易。服用他汀,也可能导致肌病、肝功能异常等副作用。
于是现实当中的情况,往往是真正吃他汀的,只有需要吃他汀的患者中的一半,而降脂达标的,又只有真正吃药患者的一半。这两次对折一打,最终的降脂达标率也就是25%而已[9]。
25%还是模拟的理想结果,真实情况可能更不容乐观(图片来源:Pixabay)
抑制PCSK9,对科学家和医生来说更是全新的领域。让PCSK9减少甚至消失,会不会有意料之外的负面影响?虽说有达拉斯心脏研究和ARIC研究受试者的资料,但这两项研究毕竟是心血管方面的,看健康还是得看整体。
Hobbs解决问题的方法还是“真人证据”,她把达拉斯心脏研究的范围更进一步扩大,从受试者的亲属当中,寻找PCSK9基因功能缺失性突变,在突变程度上更彻底的个体。在当时的条件下,这比实验室里的基因编辑可快多了。
2004年9月的一天,一位护士敲响了Sharlayne Tracy(化名)的家门。Tracy的母亲参与了达拉斯心脏研究,也同意让家人参与,因此这位被当地人叫做“胆固醇女士”的护士,就上门来给这家里的其他人做检测。
看到Tracy的初步检测结果,Hobbs团队的一位医生惊到了:她的LDL-C只有14mg/dL?“你不应该这么健康啊!”但从事健美操教练工作的Tracy,一直都“健康得像匹马”,倒觉得医生们有些大惊小怪。
在Tracy的同意下,Hobbs的团队对她做遍了大大小小的各种测试,结果没找到任何健康层面的问题。基因测序的结果则证实,Tracy同时携带了两种不同的PCSK9突变,一种还是此前未发现的,导致她体内基本就测不到PCSK9的存在。

基因变异,有时候就是这么神奇(图片来源:Pixabay)
用Hobbs的话说,Tracy简直就是个“基因敲除人”,而她的出现,相当于直接证实了抑制PCSK9降脂的安全性。“不少基因学家还没明白怎么回事,但制药巨头们直接就开动了”[10]。
研发降脂新药这么急迫,从哪个角度看都是必然的。肥胖趋势、老龄化、生活方式的不健康,会让心血管疾病的威胁越来越严峻,患者越来越多。而且就算是在中国,冠心病和中风,二十多年前也已经稳坐疾病致死人数的前两名。
具体看数据的话,2017年《柳叶刀》这个杀手排行榜上第三到第十的死因,加起来才和冠心病+中风相当[11]。这两个大反派,往往还是突然出手,大概率一击致命。患者多还致命,不重点对抗它们,对抗谁呢?

富贵病?中国人苦心血管疾病久矣(图片来源:《柳叶刀》)
抑制PCSK9的降脂药,主要是用到心血管疾病的二级预防。冠心病和中风,对患者来说往往是阴魂不散,一击不中不意味着彻底安全。管控好危险因素,才能让它们离得远一点。
降脂,就是管控危险因素的重要一环,但他汀类药物的困局,也不是靠依折麦布之类的新药能完全突破的。而以今天的眼光来看,降脂就是要大力出奇迹,把LDL-C降得越低,心血管疾病再次来袭的风险就越小[12,13]。
安全性的保证,加上临床的迫切需求,抑制PCSK9药物研发的大潮,在Hobbs团队公布ARIC研究分析的第二年,就已经报告了不少成果[8]。对征服这个靶点,许多人不约而同地选择了单克隆抗体。
阿利西尤单抗就是从这波大潮中诞生的,它在2015年7月正式被FDA批准,成为了第一个登陆美国的PCSK9抑制剂。从PCSK9作为“疑似FH致病基因”被发现,到阿利西尤单抗的获批,不多不少,又是十七年啊。
而这次在中国,经历曲折的PCSK9抑制剂,到底是以怎样的表现,投身心血管的战场呢?
艰难的旅程,才有远大的前程
阿利西尤单抗的获批依据,主要来自2018年公布结果的ODYSSEY OUTCOMES试验。这项试验的名字就很有深意了:ODYSSEY,奥德赛,荷马史诗里伟大而艰难的旅程,概括PCSK9抑制剂的过去、现在和未来,真的是恰如其分。

临床试验起名很多都是有深意的,这个话题解读开来很有意思(图片来源:Pixabay)
其实在此前的ODYSSEY试验中,阿利西尤单抗治疗心血管疾病高危患者,就已经安全地把LDL-C水平降低了60%,这也是FDA批准它上市的主要依据[14]。
但LDL-C降了,不代表着患者的死亡率也一定会降,在心血管事件方面一定会有获益[15],所以才有了目标更明确,规模更大的ODYSSEY OUTCOMES试验。
目标明确,是指ODYSSEY OUTCOMES试验选择的,是限定在入组前1-12个月发生过急性冠脉综合征(ACS),且已经接受过强化或最大耐受剂量他汀类药物治疗,但LDL-C水平仍然不低于70mg/dL,没有达到降脂目标值的患者。
规模更大,当然说的是试验人数,ODYSSEY OUTCOMES试验入组了近1.9万名患者,值得注意的是,试验中还有600多名中国患者,而他们的入组是在其他国家之后补充进行的。
在具体用药上,阿利西尤单抗的使用则是跟着LDL-C转的。试验整体的降脂目标,是把患者LDL-C降到25-50mg/dL的区间评价预后,阿利西尤单抗的治疗剂量,就会以每两周检测一次的LDL-C水平做动态调整,可能加量也可能停用。
试验的主要终点则是复合性的,包括了冠状动脉性心脏病致死、非致死性的心梗发作、缺血性脑卒中、需要住院治疗的不稳定性心绞痛这一系列主要心血管不良事件(MACE),此外还在次要终点上统计了全因死亡风险相关的数据。
要获益就要全面,阿利西尤单抗就拿出了这样的表现。试验数据显示,阿利西尤单抗的使用,在最大耐受剂量他汀治疗的基础上,还让ACS患者发生MACE的风险相对下降了15%。
而在次要终点方面,阿利西尤单抗的使用,还与治疗组患者的全因死亡风险相对下降15%相关。在降脂方面,87%的治疗组患者LDL-C的水平,达到了降脂目标值[16]!
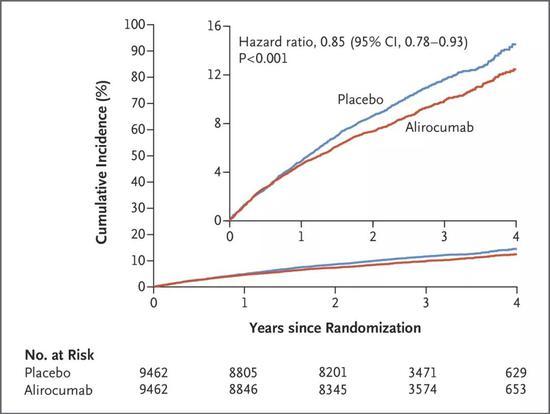
注意绝对风险和相对风险的差异啊,强调好多次了(图片来源:NEJM)
细化到每一个考量终点上,基本都能看到阿利西尤单抗的获益。治疗的安全性也相当好,不良事件发生率低,这也是抑制PCSK9的单抗类药物,目前提供的最长时间安全性证据。
治疗效果棒,安全性良好,ODYSSEY OUTCOMES试验的主要结果在2018年的美国心脏病学会(ACC)年会上公布时,就得到了高度评价,说闪耀全场毫不夸张。
最近公布的ODYSSEY EAST研究数据,也进一步体现了中国患者在接受阿利西尤单抗时,与ODYSSEY OUTCOMES试验整体相似的获益趋势,阿利西尤单抗显然也不会水土不服[16]。
踩着加速审批的“风火轮”走进中国,当然还不是阿利西尤单抗和PCSK9抑制剂的终点。精细化选择患者,搭配各种新药搭档,奥德赛的史诗旅程,这才刚刚开始呢,PCSK9的故事,肯定还能写很久很久。
参考资料:
1.Singh S, Bittner V。 Familial hypercholesterolemia—epidemiology, diagnosis, and screening[J]。 Current Atherosclerosis Reports, 2015, 17(2): 3。
2.Varret M, Rabes J P, Saint-Jore B, et al。 A third major locus for autosomal dominant hypercholesterolemia maps to 1p34。 1-p32[J]。 The American Journal of Human Genetics, 1999, 64(5): 1378-1387。
3.Seidah N G, Benjannet S, Wickham L, et al。 The secretory proprotein convertase neural apoptosis-regulated convertase 1 (NARC-1): liver regeneration and neuronal differentiation[J]。 Proceedings of the National Academy of Sciences, 2003, 100(3): 928-933。
4.Abifadel M, Varret M, Rabès J P, et al。 Mutations in PCSK9 cause autosomal dominant hypercholesterolemia[J]。 Nature Genetics, 2003, 34(2): 154。
5.Benjannet S, Rhainds D, Essalmani R, et al。 NARC-1/PCSK9 and its natural mutants zymogen cleavage and effects on the low density lipoprotein (LDL) receptor and LDL cholesterol[J]。 Journal of Biological Chemistry, 2004, 279(47): 48865-48875。
6.Jaworski K, Jankowski P, Kosior D A。 PCSK9 inhibitors–from discovery of a single mutation to a groundbreaking therapy of lipid disorders in one decade[J]。 Archives of Medical Science: AMS, 2017, 13(4): 914。
7.Cohen J, Pertsemlidis A, Kotowski I K, et al。 Low LDL cholesterol in individuals of African descent resulting from frequent nonsense mutations in PCSK9[J]。 Nature Genetics, 2005, 37(2): 161。
8.Cohen J C, Boerwinkle E, Mosley Jr T H, et al。 Sequence variations in PCSK9, low LDL, and protection against coronary heart disease[J]。 New England Journal of Medicine, 2006, 354(12): 1264-1272。
9.Cannon C P, Khan I, Klimchak A C, et al。 Simulation of lipid-lowering therapy intensification in a population with atherosclerotic cardiovascular disease[J]。 JAMA Cardiology, 2017, 2(9): 959-966。
10.Hall S S。 Genetics: a gene of rare effect[J]。 Nature News, 2013, 496(7444): 152。
11.Zhou M, Wang H, Zeng X, et al。 Mortality, morbidity, and risk factors in China and its provinces, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017[J]。 The Lancet, 2019, 394(10204): 1145-1158。
12.Navarese E P, Robinson J G, Kowalewski M, et al。 Association between baseline LDL-C level and total and cardiovascular mortality after LDL-C lowering: a systematic review and meta-analysis[J]。 JAMA, 2018, 319(15): 1566-1579。
13.Sabatine M S, Wiviott S D, Im K A, et al。 Efficacy and safety of further lowering of low-density lipoprotein cholesterol in patients starting with very low levels: a meta-analysis[J]。 JAMA Cardiology, 2018, 3(9): 823-828。
14.Robinson J G, Farnier M, Krempf M, et al。 Efficacy and safety of alirocumab in reducing lipids and cardiovascular events[J]。 New England Journal of Medicine, 2015, 372(16): 1489-1499。
15.Sabatine M S, Giugliano R P, Keech A C, et al。 Evolocumab and clinical outcomes in patients with cardiovascular disease[J]。 New England Journal of Medicine, 2017, 376(18): 1713-1722。
16.Han Y, Chen J, Chopra V, et al。 ODYSSEY EAST-A Randomized, Double-blind, Parallel Group Study to Evaluate Alirocumab Efficacy and Safety Versus Ezetimibe In High-Risk Patients With Hypercholesterolemia on Maximally Tolerated Statin in China, India, and Thailand[J]。 Circulation, 2019, 140(Suppl_1): A12214。
头图来源:Pixabay
本文作者 | 谭硕



