来源:学术经纬
褪黑素的大名,很多人并不陌生。这种天然激素可以调节人体生物钟,因此有不少人在试图改善失眠或倒时差的时候求助于非处方的褪黑素补充剂。科学家们希望针对褪黑素通路开发更安全有效、特异性强的药物帮助治疗睡眠障碍,可是褪黑素作用于受体的机制一直以来如同迷雾,给药物设计造成困难。
拨云见日的时刻终于到了!近期,顶尖学术期刊《自然》同时上线的两篇论文中,由著名结构生物学家、美国南加州大学的Vadim Cherezov教授领衔的国际团队,利用X射线自由电子激光(XFEL),首次揭示人类两种褪黑激素受体的三维结构。“我们希望把结构信息提供给其他研究人员,让他们用来设计新的药物分子或者研究患者体内这些受体的突变。”共同通讯作者Cherezov教授说。

▲两项研究的共同通讯作者Vadim Cherezov教授(图片来源:南加州大学官网)
褪黑素,调节生物钟的重要激素
在我们每个人的大脑中,有一个叫作“松果体”的结构制造和分泌褪黑素。理想情况下,随着太阳东升西落,天色亮了又暗,眼睛和大脑感知到自然光的变化,会让松果体产生的褪黑素水平随之变化,于是我们在夜幕降临后被睡意裹挟,天光大亮时欣欣然醒来。
然而,现代社会跨时区的长途旅行、夜以继日的工作安排、几乎24小时不停歇暴露在人造蓝光光源下的网络社交,我们的体内计时员难免陷入混乱。昼夜节律被扰乱的后果不可轻视,它可能导致精神、代谢、肿瘤等各种疾病。很多针对失眠、异常生理节律以及情绪障碍的药物开发便瞄准了褪黑素的两种受体。

褪黑素结合的受体有两种,MT1和MT2。过去的研究发现,人体许多部位,包括大脑、视网膜、心血管系统、肝、肾、脾和肠道都有这两种褪黑素受体。广泛的分布意味着,褪黑素的施加或缺乏会影响多项人体功能。
虽然过去的研究让科学家知道,MT1受体在控制节律方面发挥重要作用,MT2受体与体内褪黑素的周期变化活性紧密相关。但不了解两种受体蛋白更特异的差别,就很难设计选择性靶向MT1受体而不影响MT2的药物。

此时,结构生物学家对两种褪黑素受体三维结构的解析带来了新的洞见。
G蛋白偶联受体(GPCR),药物研发的“宠儿”
褪黑素受体属于一类叫作G蛋白偶联受体(GPCR)的跨膜蛋白。人体细胞已知的GPCR大约有800个,它们在细胞表面负责传递信号,对细胞的生理和病理过程都发挥重要的作用,被认为是最重要的药物治疗靶点之一。
但描绘GPCR蛋白质分子的三维结构向来是对生物物理学家的挑战。X射线晶体学是科学家们常采用的方法。这种方法往往需要蛋白质先长出足够大的晶体才能获得高分辨率的图像结构。在此次的两篇论文中,科学家们采用了独特的方法来解决生长晶体和收集X射线衍射数据的问题。
表达纯化的受体被放置在一种膜状凝胶中,由凝胶支持晶体在膜环境中生长。然后,研究人员采用一种特制的注射器,让微晶体形成一股细细的晶体流,用X射线对其扫描。得到的晶体尽管尺寸微小,但借助于斯坦福直线加速器相干光源(LCLS)的X射线,利于其超高亮度、飞秒脉冲等特性,研究人员避免了晶体在光源下受到辐射损伤的问题,成功收集到晶体数十万张散射图像,从而确定受体的三维结构。
采用同样的方法,研究人员还测试了受体数十种突变体的结构,以加深对受体工作机制的理解。
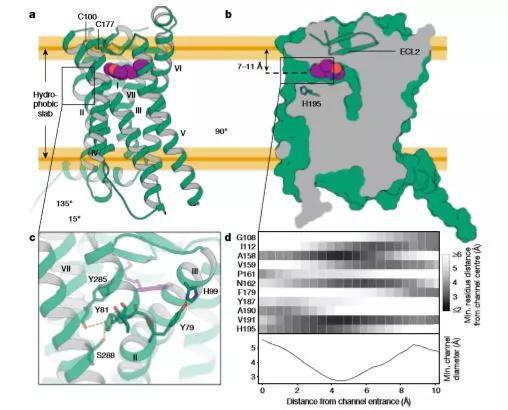
▲褪黑素受体MT1的结构特征(图片来源:《自然》)
高分辨率的三维结构显示,MT1和MT2都含有只允许褪黑素结合的狭窄通道。更有意思的发现是,比对这两个结构相似的受体,研究人员发现有些较大的化合物似乎只靶向MT1受体而不靶向MT2受体,这让设计选择性靶向MT1的药物有了可依据的基础。
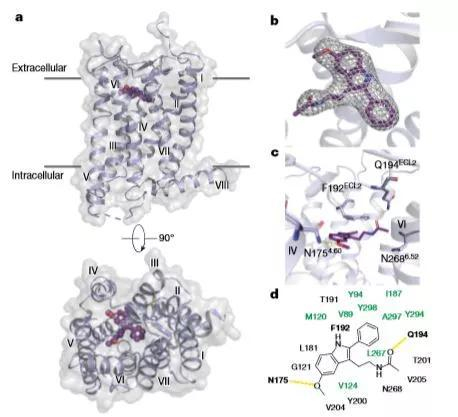
▲褪黑素受体MT2的结构特征(图片来源:《自然》)
“比较MT1和MT2的三维结构,我们能更清晰地辨析两种受体特有的结构差异,并区分它们在生物钟中的不同作用。知道这些以后,要设计出只结合一种受体的类药物分子就会更加容易。这种特异性结合非常重要,可以把不良反应降到最低。”主持MT1结构工作的通讯作者之一、亚利桑那州立大学的Wei Liu教授说。
▲夜间表达量升高的褪黑素(黑夜中的星座)与受体分子高亲和的结合促进我们的睡眠(图片来源:Bridge Institute at USC Michelson Center for Convergent Bioscience,作者Yekaterina Kadyshevskaya)
在全世界范围内,睡眠障碍影响的人群越来越大,据估计每三个人就有一人经受过短期失眠困扰。我们期待这两项研究成果能够帮助新药研发人员更快找到更安全的新型助眠药,帮助更多人获得甜美的睡眠。



