来源:奇点网
说起T细胞,大家应该不会陌生,抗病毒抗肿瘤等等免疫过程中,都少不了T细胞的身影。最近大火的肿瘤免疫治疗,无论是PD-(L)1抗体还是CAR-T,基本上都是在T细胞上做文章,准确来说是T细胞中的细胞毒性T细胞(CTL)。
可以说,CTL细胞的“死亡之吻”就是这些叛变细胞的末日。
近日,纪念斯隆-凯特琳癌症中心的Fella Tamzalit和Morgan Huse等发现,CTL细胞的这一“死亡之吻”竟然是舌吻,它会在与靶细胞的接触面上伸出很多凸起。甚至不需要穿孔素,单依靠这些凸起,CTL细胞就能在靶细胞上捅出个大窟窿。相关研究发表在Science Immuology上[1]。

细胞毒性T细胞的职责,就是去杀死那些癌变了,或者被病毒感染而“坏掉”的细胞,就像这样:
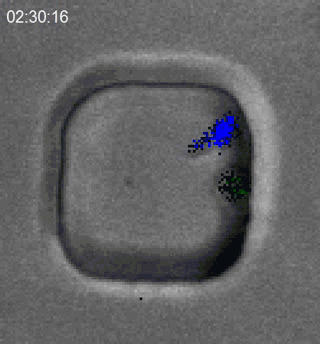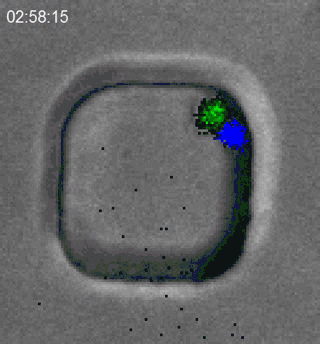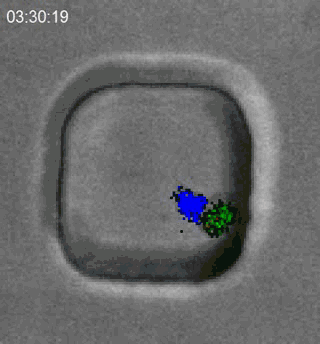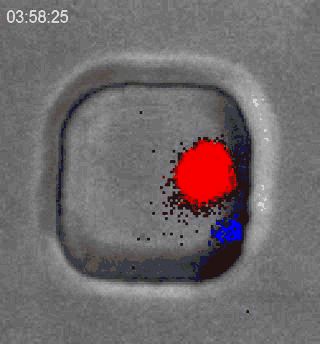
T细胞(蓝)追捕淋巴瘤细胞(绿),而后培养基中的PI与淋巴瘤细胞胞质中的RNA结合发出红色荧光
当然,这些坏掉的细胞不会自己送上门来,CTL细胞自己也要有强大的运动能力,来巡逻和抓捕这些“罪犯”。
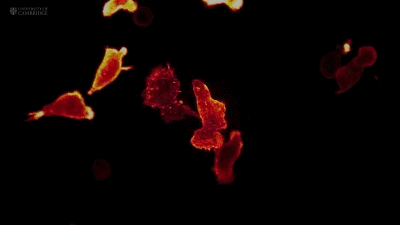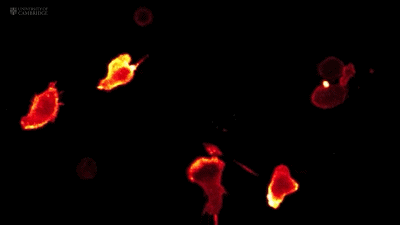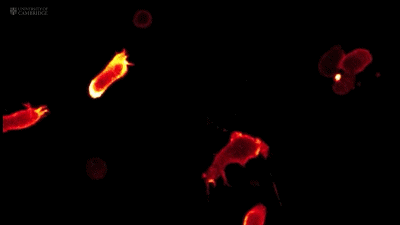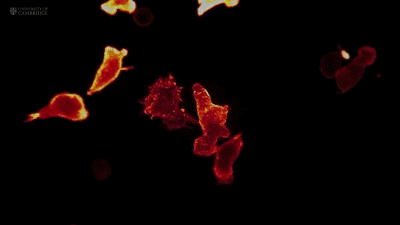
CTL细胞跟猫一样,也是流体
一旦CTL细胞通过表面的T细胞受体(TCR)找到了“坏掉”的组织细胞[2],死亡之吻就开始了。
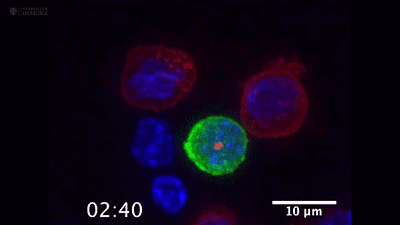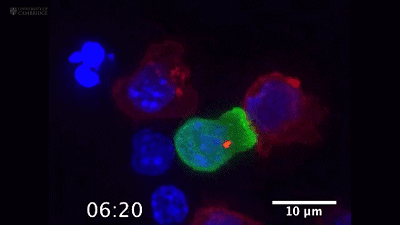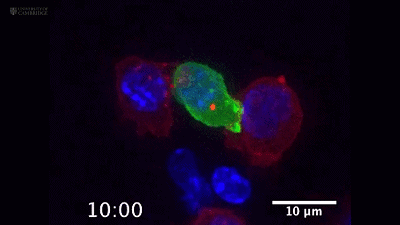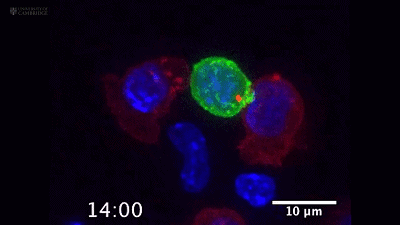
CTL细胞一口亲了上去
首先,CTL细胞的中心体向着靶细胞移动。
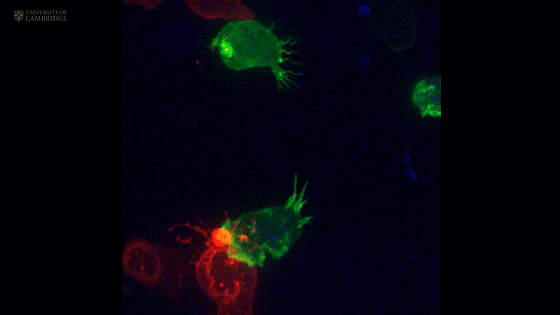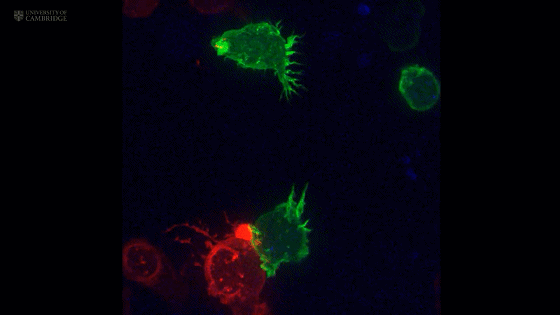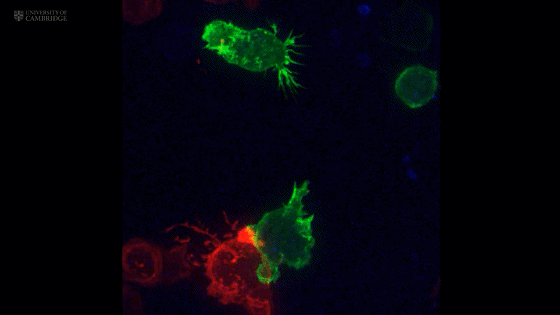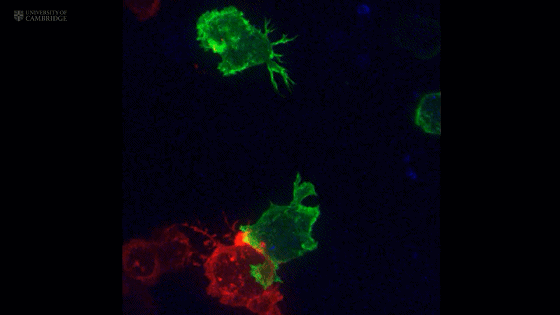
CTL细胞(绿色)和靶细胞(红色)接触后,中心体(蓝色)向着靶细胞移动
随后,中心体发出的微管把CTL细胞携带的细胞毒性颗粒也拉向了靶细胞[3]。
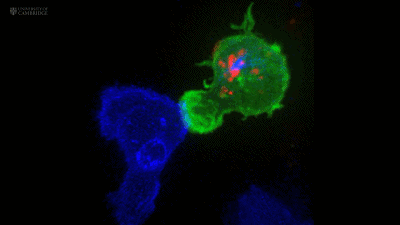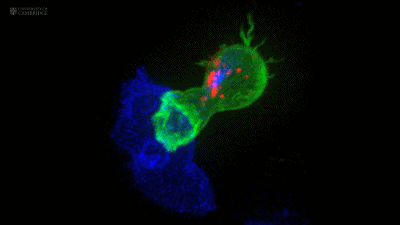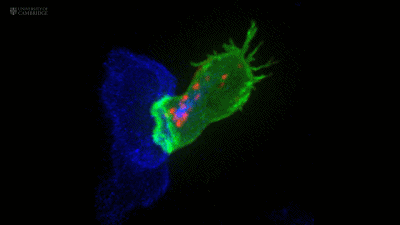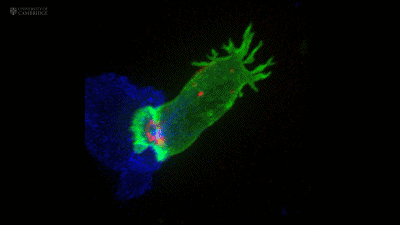
红色的就是细胞毒性颗粒
细胞毒性颗粒中主要有两种成分——穿孔素和颗粒酶[4],其中穿孔素在靶细胞表面形成孔道,而颗粒酶从中进入并杀死靶细胞。

穿孔素形成的孔道,感觉有点像导弹发射井,或者福建土楼?
干掉这个靶细胞后,CTL细胞拔*无情,转身去寻找下一个目标。

不过,2013年的一项研究却显示,抑制住毒性颗粒向靶细胞的移动,似乎并没有减弱CTL细胞的杀伤能力[5]。莫非T细胞的杀伤过程中还有别的机制?
此前,Morgan Huse等的研究就发现[6],CTL和靶细胞之间可不是简单的贴在一起,似乎在急不可耐地要把靶细胞的细胞膜扒开。这不,用来模拟靶细胞的微柱阵列中的微柱,就被CTL细胞扒的东倒西歪的:
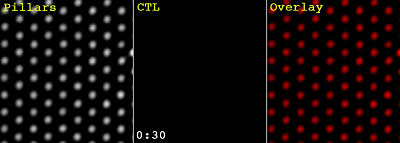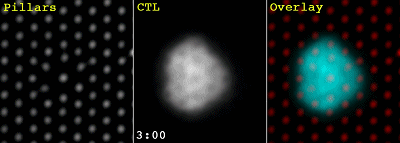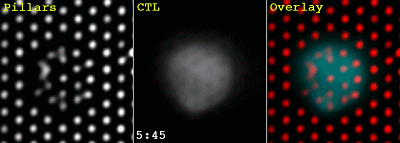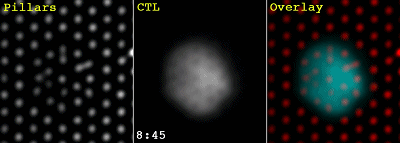
这回,研究人员进一步研究了免疫突触中的机械力的作用。
其实在微柱阵列上,CTL细胞除了把微柱扒拉的东倒西歪,还向微柱间的空隙伸出了许多凸起:
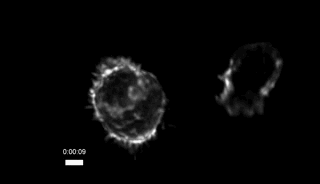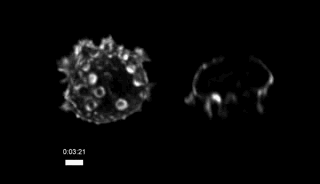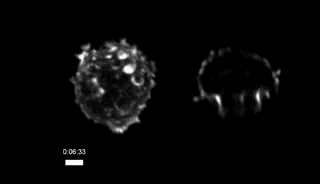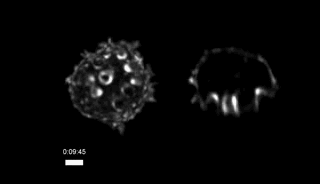
CTL细胞向微柱间伸出的凸起,微柱未显示
在真实的靶细胞上就是这样:
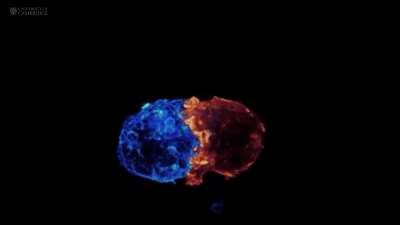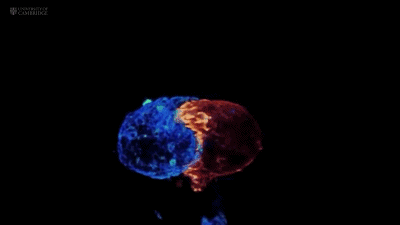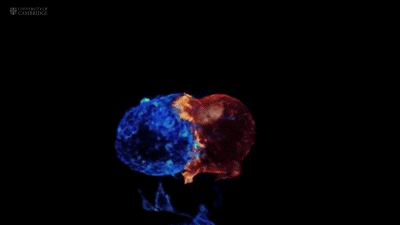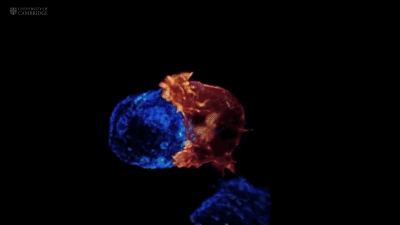
而细胞毒性颗粒的释放,也正发生在这些凸起之间:
一闪而过的蓝色荧光就是细胞毒性颗粒释放的瞬间
然后,靶细胞上就被开了个窟窿:

甚至缺乏穿孔素的CTL细胞,单纯依靠表面凸起,也能在靶细胞上捅出个窟窿

之前CTL细胞扒拉靶细胞的细胞膜,莫非是在“叩开牙关”
但要是使用Arp2/3抑制剂CK666抑制微丝的组装,进而抑制凸起的形成,T细胞对靶细胞的裂解能力却明显下降了。

CK666作用下,T细胞对靶细胞裂解能力明显下降
其实,T细胞上类似的凸起早就被发现了[7],被认为可能在抗原扫描、信号传达和细胞运动上有一定的作用。在T细胞传出血管进入组织时,就是依靠类似的凸起挤开血管上皮细胞,钻出血管壁的。没想到T细胞的杀伤过程也是通过这些凸起完成的,真是简单粗暴。



