来源:科研圈
大约 500 年前,瑞士医生帕拉塞尔苏斯提出“剂量决定毒性”的观点,这句话成为现代毒理学的基本法则。对绝大多数有毒的物质而言,剂量越大,毒性自然也越高。然而,从上世纪 70 年代起,生物学家逐渐发现,某些化学物质似乎拥有与众不同的特性:在剂量非常低的情况下,反倒具有更大的毒性。然而,直到现在,各国监管机构仍然鲜有制定相应法规,对此类化学物质进行足够的管制……
帕拉塞尔苏斯(Paracelsus)是16世纪一位性情暴躁的医生,一生游走于欧洲中部的各大城镇,在治疗中大胆使用水银、鸦片及其他危险药物。他那显得有些冒险的医疗理念,与当时施行放血术的医生和传统医师大不相同。他曾在晚年所写的书中,为自己采用的非传统疗法进行辩护:“所有东西都含有毒素,没有任何东西是完全无毒的:剂量才是决定物质毒性的关键。”在几个世纪后的今天,帕拉塞尔苏斯那些在当时被认为是极端的看法,已经得到了广泛认可,他的话也可以被精简为:“剂量决定毒性”,而这正是现代毒理学的基本法则。
内分泌干扰物:争议渐起
帕拉塞尔苏斯的这句名言使他成为了毒理学之父。现在对于这一观点的解释是:毒性与剂量呈线性变化关系,因此减少有害物质的剂量,可以降低风险。这一观点不但是一个抽象化的哲学表述,更是 20 世纪中叶兴起的化学物质安全测试的基本前提。风险评估人员一般会看,当一种化学物质的剂量很高时,会对人体产生什么不良影响,然后据此进行推断,制定该物质的安全标准。而这些都基于一个前提:有毒的化学物质在低剂量时,其毒性会大幅降低。

毒理学之父帕拉塞尔苏斯
但是,如果帕拉塞尔苏斯的假设是错误的,会怎么样呢?假如有一类强效的化学物质在低剂量下,对人体的危害更大,那又怎么办呢?越来越多的科学研究人员宣称,内分泌干扰物(endocrine disruptor)就是这样一类化学物质,一般的毒理学无法完全解释其毒性。这类物质会与细胞激素受体(cellular hormone receptor)发生反应,比如广泛使用的除草剂莠去津(atrazine)、塑化剂双酚A(bisphenol A,BPA)、清洁剂中的抗菌剂二氯苯氧酚胺(triclosan)以及葡萄园中使用的杀真菌剂中的烯菌酮(vinclozolin)。监管机构根据常规的大剂量测试(high-dose testing),对这些化学物质的使用剂量设定了安全上限,认为低于上限的剂量对人体就是安全的。但研究人员却发现,一些存在于日常环境中的极其微量的化合物,其毒性实验数据并不符合经典的毒理学“剂量-反应曲线”。相反地,大多数内分泌干扰物所呈现的则是U形,或倒U形,甚至波浪形。
费雷德里克·沃姆·萨尔(Ferderick vom Saal)是美国密苏里大学哥伦比亚分校的神经生物学家,他从20世纪70年代起就告诫人们,警惕内分泌干扰物对人体的影响,“我们目前所测试过的每一种内分泌干扰物都具备复杂的剂量-反应曲线,我估计所有此类化合物都是如此。而传统的毒理学方法则完全无法预测这类内分泌干扰物质在低剂量下的毒理表现”。

在上世纪70年代,萨尔就告诫人们,警惕内分泌干扰物对人体的影响。
萨尔及其同事认为,环境中所存在的微量内分泌干扰物质,是造成各种人类健康问题(包括肥胖、糖尿病、癌症、心血管疾病、不育以及其他与性发育相关疾病)的元凶。
然而,很多毒理学家对此并不信服,特别是那些在工业界或政府部门从事传统风险评估的毒理学家。虽然他们也承认,内分泌干扰物质的确具有一些奇特的毒理性质,但他们表示,萨尔和其他持类似观点的研究人员所进行的研究,还没有得到重复实验的证实,而且过度依赖未经验证的检验方法,过于注重那些并不会给人体带来明显危害的症状,比如器官重量、癌前增生、基因和蛋白活性的变化等。美国Gradient环境咨询公司毒理学家、美国化学委员会顾问洛伦茨·龙伯格(Lorenz Rhomberg)说:“如果要我们相信低剂量内分泌干扰物质对人体健康的影响,他们就必须拿出证据,证明他们的实验结果是可重复的,证实这种现象不是仅出现在某个研究人员的某一次实验中,而是经得起科学检验,真正会对人体造成不良影响的毒理现象。”
萨尔及其同事对这些质疑的回答是:内分泌干扰物质的研究在迅速发展,他们现在已经能提供龙伯格所要求的系统性证据。2012年发表的一篇综述,对迄今该领域中的600多项研究进行了一次全面总结(几乎包括了他们该领域5年来发表过论文的一半),并发现有可靠证据显示,18种内分泌干扰物质(包括BPA、莠去津及烯菌酮)在低剂量下会不同于传统的剂量反应,危害人体健康。这篇综述的主要作者、现任美国马萨诸塞大学安姆斯特分校助理教授的劳拉·范登堡(Laura Vandenberg)说:“质疑我们研究结果的科学家,一直在指责我们没有足够的证据证明这个现象的真实性,现在我们接受他们的挑战。”
欧洲和美国的政府官员对这个研究领域也十分关注。美国国家环境卫生科学研究所所长琳达·波恩鲍姆(Linda Birnbaum)认为,“范登堡的综述很具说服力,也十分可信”。2012年,波恩鲍姆在NIEHS旗下的《环境健康展望》(Environmental Health Perspectives)杂志中提出,“现在,应该是时候讨论一下该不该将化学物质的低剂量反应纳入监管决议了”。
时任欧盟环境总署化学品部负责人比约恩·汉森(Björn Hansen)透露,2012年6月,在比利时布鲁塞尔召开的欧盟科学会议上,与会代表们虽然无法就低剂量反应的重要性达成一致意见,但都同意有必要加强现有法规。与此同时,美国环境保护局(EPA)和食品及药品管理局(FDA)也表示,愿意就该问题展开讨论,但他们认为目前大规模的法规修订还言之过早。
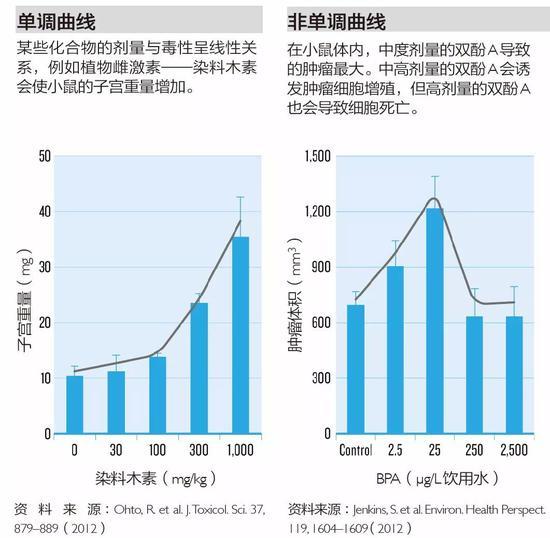
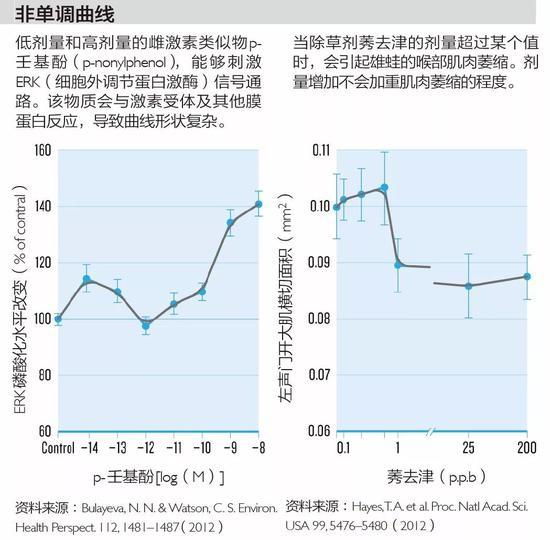
研究人员发现,许多内分泌干扰物的“剂量-反应曲线”不同于一般药物的单调曲线。
独特的毒性曲线:不可小觑低剂量
自从有关内分泌干扰物的纷争存在以来,萨尔就一直处于争论的中心。20世纪70 年代,萨尔在美国得克萨斯大学奥斯汀分校做博士后研究时,就吃惊地发现小鼠子宫里性激素水平的细微变化,会对其中的胚胎产生终身影响。在子宫中处于两只雄鼠胚胎之间的雌鼠胚胎,与处于两只雌鼠胚胎之间的雌鼠胚胎相比,成年后表现出的“雄性化”特征(如攻击性)明显强于后者。显然,这是相邻雄性胚胎释放的微量睾酮造成的。
萨尔首先对天然激素和合成雌激素己烯雌酚(diethylstilbestrol,DES)进行实验。他发现,与未接触过DES的雄鼠相比,在出生前接触过微量DES的雄鼠,其前列腺更重,后来更易患包括癌症在内的前列腺疾病。但奇怪的是,更高剂量的DES却不会造成这些影响。己烯雌酚是最早被发现具有非单调“剂量-反应曲线”的内分泌干扰物之一。其后,萨尔与密苏里大学的同事韦德·威尔休斯(Wade Welshons)发现,多种内分泌干扰物都具有类似的非单调反应,特别是BPA。
萨尔的早期研究引起了国际上对BPA的关注,并成功促使美国、加拿大和一部分欧洲国家停止在婴儿奶瓶和幼儿水杯的制造中使用BPA。研究还激发了大批研究人员,对低剂量BPA及其他合成激素对动物的内分泌影响展开了更深入的研究。例如,塔夫斯大学的细胞生物学家安娜·索托(Ana Soto)就发现,过早接触BPA,会影响大鼠和小鼠的乳腺发育,促进雌激素受体的生长,导致癌前增生及癌症。另一位细胞生物学家,西班牙米格尔·赫尔南德兹大学的安杰尔·纳达尔(Angel Nadal),通过向人工培养的人类胰腺细胞施加BPA,发现了BPA剂量水平和葡萄糖代谢变化(糖尿病和肥胖的风险因子之一)之间的非单调关联性。流行病学家也加入这场论战中来。他们发现,尿液中的BPA 水平与儿童肥胖具有一定的关联性,并将其他内分泌干扰物与糖尿病的发病率联系起来。
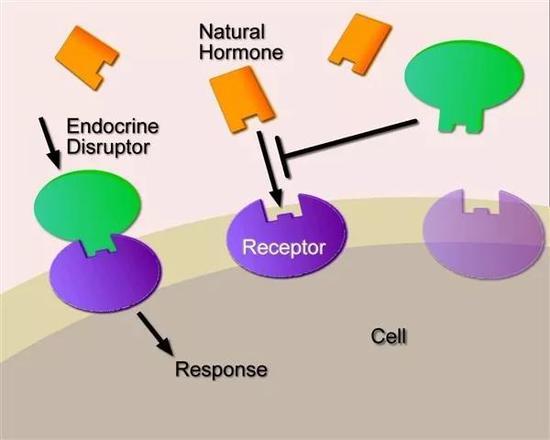
BPA与雌性激素受体结合示意图
他们的研究向人们展示了一个内分泌干扰的奇异世界,它与传统毒理学完全不同,就好像量子力学与经典物理学完全不同一样。在动物发育的关键时期,即使只是极微量的BPA和其他干扰物与激素受体发生反应,也会影响受体的正常功能,产生难以理解的实验结果,特别是当其他激素也参与其中时。
这类激素受体间的相互影响,会产生异常的“剂量-反应关系”,其中很多关系,科学家还在努力阐明。2012年10月,萨尔在密苏里大学的研究小组首次发表了一种广泛使用的塑料成分——DEHP(一种邻苯二甲酸酯)的非单调“剂量-反应曲线”。这个研究小组对78只怀孕小鼠施加不同剂量的DEHP,然后监测不同剂量的影响。这次实验使用的剂量跨度极大,从0.5微克/千克体重/天直到50万微克/千克体重/天。
实验发现,根据DEHP施加剂量的不同,小鼠的睾酮水平及其性发育会出现令人惊讶的变化。举例来说,雄性小鼠的实验曲线看起来像起伏的山峦。在0~0.5 微克的剂量之间,小鼠血清中的睾酮水平随剂量的增加上升,但到1微克的剂量时,小鼠血清中的睾酮水平则稍微下降;接着从5~500微克之间,又呈上升趋势;当DEHP的剂量达到5万微克时,睾酮水平又开始下降;在50万微克剂量时,则开始迅速下降。实际上,最高剂量下的睾酮水平与未施加DEHP的对照组水平相同。为避免遭到质疑,萨尔对实验数据进行了吻合度 (goodness of fit)的统计分析,结果证实非单调曲线最符合实验数据。
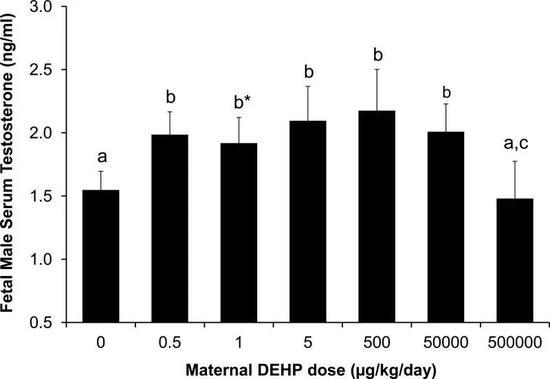
该实验中,DEHP剂量与小鼠睾酮水平的关系
DEHP的怪异曲线背后,隐藏着一个未知的生化机理,要阐明这个机理还有待进一步研究。不过,研究人员已经找到了其他非单调曲线的确切成因。其中,科学家了解得最透彻的一个例子并非污染物,而是一种药物——他莫西芬(tamoxifen)。这种化疗药物会与乳腺细胞中的雌激素受体结合,“剂量-反应曲线”呈倒U形。极低剂量的他莫西芬不仅不会抑制癌细胞,而且随着药物在乳腺细胞中慢慢累积,还会刺激肿瘤生长,导致病人进入一个痛苦的爆发期。当他莫西芬在组织中的浓度进一步增加,直到足以与其中所有的雌激素受体结合,才会开始抑制癌细胞的生长。美国马萨诸塞大学阿姆赫斯特分校的托马斯·策勒(Thomas Zoeller)说:“内分泌学家对这个过程十分了解,非单调剂量反应是一个无可争辩的事实。”
2009年,美国内分泌学会发表的一份科学声明,标志着该研究领域的一个转折点。这是该学会在其95年的历史中,发表的第一份科学声明。其中指出,“内分泌干扰物是公共卫生的一个重大隐患”,该学会支持加强管制,认可非单调剂量反应,并表明“即便是极微量的接触,只要有接触,内分泌干扰物就有可能导致内分泌或生殖异常”。2011年,另外7个科学团体与内分泌学会一起,在《科学》杂志上发表一封联名信,表达对该问题的关切。加利福尼亚大学欧文分校的分子生物学家布鲁斯·布隆伯格(Bruce Blumberg)说:“这份声明肯定了内分泌干扰物研究的主流地位,从根本上转变了该领域的命运。”

美国的12个州已经禁止将BPA用于儿童水杯的生产
巨大的分歧:何时纳入监管?
然而,科学评论家却认为,非单调反应和低剂量效应存在与否并非问题的关键,最重要的问题是,它们对人体健康到底有多大影响。美国FDA食品安全和应用营养学中心的毒理学家杰森·昂斯特(Jason Aungst)认为:“非单调性确实存在,但问题是它是否真的具有毒理学意义。”他和一位在EPA 工作的资深毒理学家厄尔·格雷(Earl Gray)认为,萨尔、索托和其他研究者所发现的低剂量效应,还是一个相对罕见的现象,不足以确定该现象与主要健康问题的关系。
学者对于该问题的意见分歧如此之大,一定程度上是由于研究人员与风险评估机构采用了不同类型的测试方法。制药厂商为获得上市批准,通常会雇用私营检测机构测试新产品,但这类实验室通常没有能力检测极低浓度的化学物质。这些私营机构通常不会检测药物引起的复杂生化改变,例如蛋白质水平的变化,而这正是策勒、索托及萨尔的实验室所做的常规检测之一。相反,监管机构规定的标准化检测,要求检测方法更简单、更容易重复;检测更多实验动物;针对更明显的健康问题,如急性毒性、癌症和身体畸形。
然而,就算政府机构和工业界的科学家想要找到低剂量效应,通常也一无所获。例如,格雷和任职于RTI国际的发育毒理学家罗谢尔·泰尔(Rochelle Tyl)就对BPA的低剂量效应进行了研究,但并没有发现萨尔等研究者所证实的严重发育影响。萨尔与其同僚则反驳,泰尔和格雷的研究没有发现BPA的低剂量效应,是因为他们施与阳性对照动物的雌二醇剂量过高。
由于泰尔和格雷的研究结果不理想,FDA和EPA都没有更改它们对BPA的风险评估。FDA仍然坚持50毫克/千克体重/天的BPA剂量对人体没有不良影响,而萨尔却认为BPA的安全剂量范围应该比这低200万倍,即25毫微克以下。然而,目前这两个监管机构正合作展开一项大规模的研究,以解决这场纷争。这个由NIEHS和FDA国家毒理研究中心牵头的新项目,耗资2000万美元,它是迄今为止,针对非单调剂量-反应毒理曲线进行的规模最大的研究。2012年9月,研究人员开始给大约1000只小鼠喂食5个不同剂量的BPA,测试范围从2.5微克/千克体重/天,到2.5万微克/千克体重/天,并采用了两个阳性对照组(所施与的雌二醇量远低于泰尔或格雷所采用的)和一个阴性对照组。萨尔、策勒和其他学者将会参与组织分析,测量一系列标准监管测试中没有检测的健康影响,例如前列腺和乳腺组织生理代谢的变化。
这项大型BPA研究目前仍在进行中。在2015年发表的中期报告中,低剂量的BPA已经显现出了一些危害。研究团队预计,最终结果将于今年发布。而萨尔在实验室中,也找出了更多关于BPA毒性的证据:在2014年发表的一篇论文中,萨尔首次发现了低剂量BPA对哺乳动物器官发育的副作用。2017年1月,欧盟将BPA列入“高度关注物质”(SVHC)的候选目录,朝着禁止进口、使用BPA跨出了第一步。
而在更多研究结论出炉之前,这个研究领域的一些资深科学家决定不再等待,他们合写了一篇论文,就如何检测新合成的药物对内分泌的影响,以及如何检测这些在低剂量下的非单调“剂量-反应曲线”,向工业界的化学家给出详尽的建议。论文还附有一个相关的网站,它致力于避免可能有害的内分泌干扰物流入市场。
萨尔希望这项举措有助于给监管机构施加压力,限制市场上的有害化学物质。他解释道:“我们只是要告诉制造商,如果你们希望研制安全的化合物,就应该这样做。我想这无可非议。”



