来源:赛先生
撰文 | 李研
责编 | 刘睿 李珊珊
磷的发现极具传奇色彩。
1669年的一个夜晚,在德国汉堡圣米迦勒教堂(St。 Michael‘s Church)的地下室里,一位名叫波兰特(Henning Brand)的炼金术士正试图从尿液中获取“哲人石”。和当时其他笃信炼金术的人一样,波兰特热衷于寻找这种能够将廉价金属变为贵重黄金的神奇物质。至于为什么匪夷所思地选择了尿液,据说是因为他觉得人体本身就很神奇,从嘴巴吃进去的跟排泄出来的物质完全不一样,而尿作为人体液的一种,颜色又和黄金有那么点接近,没准就是成功的关键呢。在当晚的实验中,他将砂、木炭、石灰等和尿混合,加热蒸馏。这一次,他的虔诚之心似乎得到了回报,一种带有蜡状白色固体意外出现了。这种物质在幽暗的地下室里,竟然不需加热就能发出美丽的光。
波兰特马上意识到自己发现了不寻常的东西。他最初把这种物质叫做kalte feuer(德文意为冷火),后来又称之为“phosphorus”。这个名字由”phos”(光) 和”phorus”(承载者)组成,意为“光的载体“。
世界上知名的油画不可胜数,但约瑟夫·怀特(Joseph Wright)在1771年完成的《炼金术士发现磷》是屈指可数的以化学新发现为素材的名画。画家用生动而夸张的笔触重现了科学史上那个重要的时刻——波兰特目光炯炯,虔诚地注视着蒸馏瓶中醒目的光辉。

The Alchemist Discovering Phosphorus (1771) by Joseph Wright 。这幅画的完整标题是:“寻找哲人石的炼金术士发现了磷,他在祈祷自己的操作可以成功,就像古代化学占星术士的笔记一样。” 图源:Wikipedia
该发现使波兰特不仅成为发现磷元素的第一人,还无意间成为化学史上有记录的第一个发现新元素的人。之前已知的化学元素(如金、银、铜、铁等)因为很早就应用在生产和生活中,并没有明确史料记载它们的发现者。
然而,那时的人们对化学元素的概念还一无所知,波兰特本人也没有意识到自己发现的科学意义。作为一个还有些商业头脑的人,他起初打算严守机密,期待从这种奇特发光物质中获利。遗憾的是,这种发光物质并不是他设想的能够点石成金的“哲人石”,而且由于具有强烈的臭味又极为易燃,也难以取代蜡烛用于室内照明,似乎没有半点用处。于是,他只能靠偶尔透露这种发光物质的一些细节来换点小钱。消息不胫而走,德累斯顿一位名叫克拉夫特(Daniel Kraft )的商人成功说服波兰特以很低的价钱出售了从尿液制磷的方法,而后转手在欧洲广泛传播,获利颇丰。只是不知道波兰特得知后会作何感想。
在波兰特发现磷大约10年后,作为近代化学的重要开创者,英国化学家波义尔(Robert Boyle,1627-1691)借助从德国获取的消息,成功复制了从尿液中提取磷的实验。随后他将磷的制备方法以及磷的一些性质公之于众。
在波兰特发现磷50年后,一位名叫约翰·亨欣(Johann Thomas Hensing)的德国药剂师又在人脑中提取出同样的物质。因为大脑中含有磷,18世纪初的一些人曾将磷视为类似“脑白金”的补品。然而,随意服用含磷药物不仅不能补脑,还往往会导致磷中毒。
波兰特发现磷100年后,瑞典科学家又发现磷还广泛存在于人和动物骨骼中,将硫酸和骨灰放在一起加热也可以得到磷。这让磷的获取变得更加容易。
随着元素概念的发展,到了1796年,法国著名化学家拉瓦锡(Antoine-Laurent de Lavoisier,1743-1794)终于认识到波兰特提取的发光物质是一种元素。Phosphorus这一名字被沿用,磷(元素符号P)自此正式成为元素家族中的一员。
多变的磷
波兰特当年发现的磷是白色蜡状固体,但磷原子通过不同的排列方式,还可以变身为红色粉末,或者带有金属光泽的黑色固体等多种形态。化学家把这些由同种元素组成,但化学和物理性质并不相同的物质称为同素异形体。
磷常见的同素异形体包括白磷、红磷和黑磷等几种。

白磷(左)、红磷(中)和黑磷(右)的形态及分子结构 图源:Wikipedia
白磷是一种白色或浅黄色半透明态的固体,分子式为P4,其中四个磷原子通过六根P-P键形成正四面体结构。分子结构具有很强的张力,导致白磷的反应活性很高,在室温下就可以与空气中的氧气反应,并发出冷光。
白磷十分易燃,着火点只有大约40 ℃,在受到摩擦、撞击或氧化时都有可能导致局部温度达到着火点,从而引发“自燃”。人们将白磷、硫和树胶等混合物涂裹在小木头棒上,只要在粗糙的物体表面进行摩擦后即可生火,这便是最初的火柴。但这种火柴有两个显著缺点:一是白磷对人体有剧毒;二是太过易燃导致使用起来不够安全。
1845年,奥地利化学家施勒特尔(Anton Schrötter von Kristelli)发现了磷的第二种同素异形体——红磷。红磷中多数磷原子为链状排布,活性比白磷低,室温下不会和空气中的氧发生反应,也就不会发光或者自燃。
红磷的着火点约为240 ℃,比白磷高出许多,再加上红磷基本无毒,人们开始用红磷替代白磷制作更为安全的火柴。现代的火柴,一般将红磷涂在火柴盒侧面,当火柴头上的氯酸钾等易燃物质在火柴盒两侧摩擦时,就因接触红磷并发热而点燃。在打火机问世之前,红磷制成的火柴是人们日常取火的主要手段。

含有红磷的火柴盒。图源:Wikipedia
至于磷的另一种同素异形体黑磷,可通过白磷或红磷在高温高压作用下转化而成。它的反应活性更低,表面具有类似黑色金属的光泽。虽然磷本身是非金属元素,但黑鳞由于特殊的原子层状排列方式却可以传导电流,能够制作成半导体材料。而且,用类似从石墨中获取石墨烯的方法,从黑磷中也可以得到黑磷烯纳米片。伴随着近年来人们对半导体和二维材料的日渐重视,黑磷这种不易燃不发光、几十年前还鲜有人知的磷单质, 如今已成为材料科学中一颗冉冉升起的新星。
黑磷烯具有很高的比表面积和优异的光电特性,但致命的缺陷是稳定性差。当接触水和氧气时,黑磷片层极易被氧化分解。近年来,国内一些研究团队在高稳定性黑磷的制备方面取得了突破,预计可有效推动黑磷在能源、催化和生物医学等领域的广泛应用。
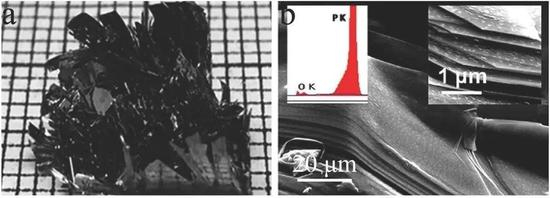
(a)黑磷的外观带有金属光泽(图源:参考文献4 );(b)在扫描电镜下,黑磷具有的纳米 层状结构 (图源:参考文献5)
生命的必需元素
磷首次发现于人的体液,磷也与我们的生命活动息息相关。
人体内,磷大约占体重的十分之一,其中80%是与钙结合、以磷酸盐形式支撑着我们的坚硬骨骼和牙齿。其余的磷与蛋白质、脂肪、糖等结合形成有机物,在细胞膜发育、能量交换以及很多关键的生理过程中发挥着重要作用。
特别是,当磷酸盐形成两个酯键时,就会构成磷酸二酯键,而磷酸二酯键是核酸骨架的重要组成部分。从复杂的人体到微小的病毒,已知的所有生命形式都离不开核酸,因为核酸负责着生物体遗传信息的携带和传递。
自然最终选择磷及磷酸二酯键构成遗传物质的骨架是有原因的。了解有机化学的读者都知道,酯类通常并不是一种非常稳定的功能团,在中性水溶液中,普通的碳酸酯(例如乙酸乙酯)最多只能稳定数月。而一个遗传基因片段中就含有几千个磷酸二酯键,如果它们经常发生断裂水解,生命将不太可能稳定存在。
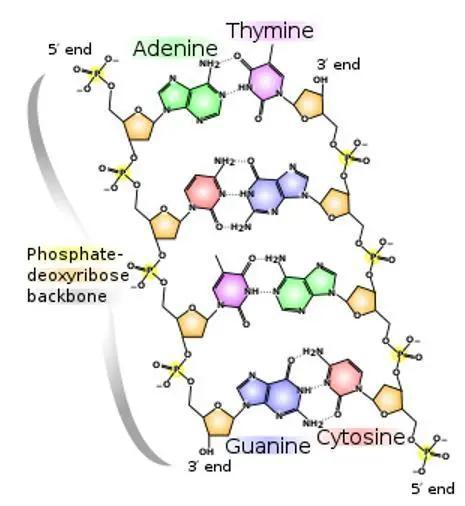
脱氧核糖核酸(DNA)的化学分子结构。图源:Wikipedia
然而,磷酸二酯键具有非常特殊的结构,它在生理pH值条件下可以带有负电荷,由于同种电荷之间的相互排斥,溶液中带负电的亲核基团(Nu)就难以进攻磷酯键,从而大大提高了结构的稳定性。在不太苛刻的自然条件下,脱氧核糖核酸(DNA)可以保存近百年。如果将其小心冷冻起来,更是可以存放千年之久。
更重要的是,磷酸二酯键的稳定是相对的。在适当条件下,带正电的金属离子或多胺化合物可以中和负电,这时磷酯键可以被亲核试剂轻易打开,完成生命生长和繁衍所必须的各种化学反应。
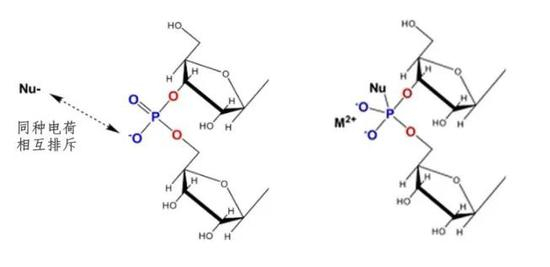
核酸这类复杂的生物大分子,得益于磷酸二酯键的支撑,能够在亿万年中稳定又不失活力的作为遗传信息的载体,可谓大自然在生命深处留下的鬼斧神工。
生命的限制元素
我们很难找到可以取代磷独特作用的元素,所以磷与碳、氢、氧、氮、硫一起被认为是生命组成必不可少的元素。[注2]然而,相比于其他5种必需的元素,磷在地球上的储备并不十分丰富,未来甚至还有“断供”的风险。
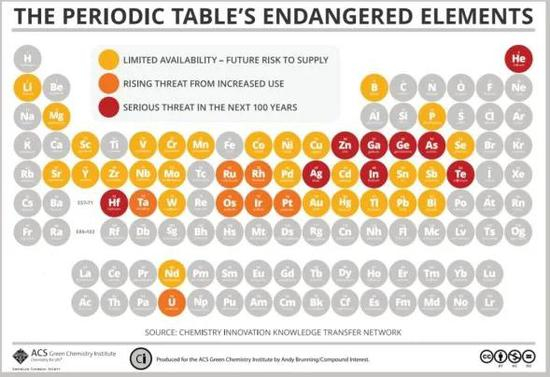
美国化学会(ACS)制作的显示各种元素稀缺程度的周期表。P是生命必需元素中唯一具有短缺风险的。
人类为什么需要这么多磷?要知道,庞大并且还在日益增长的世界人口每天消耗着大量的粮食,而氮、磷、钾是农作物生长需求量大、收获时又带走量较多的三种营养元素,所以长期耕种的土地很容易缺乏,必须人工施肥补充才能保持高产。这其中,人们已经掌握了将空气中的氮气转变为氨的人工固氮法,所以氮肥是最不用发愁的。磷和钾都只能从地壳中获取,而钾的来源和储量又比磷丰富得多。如今人们早已抛弃了蒸馏尿液获取磷的方法,制造农用磷肥的主要原料是磷灰石。根据美国地质调查局2015年的统计,全球可供商业开采磷矿石储量为670亿吨,但摩洛哥和西撒哈拉这一小块区域就占据了500亿吨之多,中国有近40亿吨,大多数国家的磷矿资源比较匮乏。
另一方面,目前的农业技术又使磷的流失率高得惊人,撒到地里的磷肥只有约10%可以被农作物吸收利用,剩下流失到水体中的磷还会对环境造成严重污染。
按照现有的开采速度和利用方式推算,地球上磷矿石的商业储量可能在50年后消耗殆尽。因此,科学家们正在积极寻找从有机废物和生活废水中高效回收磷的方法,以应对磷矿石未来可能出现的短缺。
虽然地球上的磷资源似乎不能满足人类的巨大需求,但在浩瀚宇宙中,我们生活的地球已经是个十足的“幸运儿”了。天文学家发现,太空中磷的含量远低于我们的想象,像地球这样富含磷元素的星球在银河系实属凤毛麟角。为什么地球可以得天独厚地享有大量的磷资源,目前科学家对此尚无可靠的解释。但可以肯定的是,磷在早期生命演化中发挥着不可或缺的作用,如果星球表面没有它,生命可能根本不会出现。这或许可以解释为什么我们发现了一些温度和水分都理想的“宜居星球”,却始终难觅外星生物踪迹。
可见,磷不仅是生命的必需元素,更是生命的“限制元素”。
“生存本来就是一种幸运,过去的地球上是如此,现在这个冷酷的宇宙中也到处如此。但不知从什么时候起,人类有了一种幻觉,认为生存成了唾手可得的东西,这就是你们失败的根本原因。”
——《三体3》
死亡烟火
科学上的每项新发现往往都是双刃剑,在给人们带来福祉的同时也常会引发风险和灾难。磷的使用也不例外,它既能给世间带来生命和丰收的喜悦,也能散布死亡和恐怖的威胁。
白磷的燃点低,极易引燃其他物质,所以白磷引发的火灾往往很难扑灭。白磷燃烧时会急剧放热,并产生浓浓的白烟。白烟的成分为五氧化二磷(P2O5),实际分子结构为P4O10(P2O5是约分简化的结果)。接触白磷或者吸入其燃烧产生的烟雾都会对人造成严重伤害。
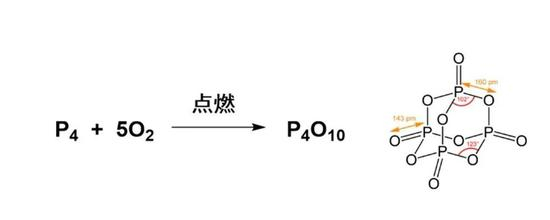
白磷燃烧的化学方程式和五氧化二磷的分子结构
很快,白磷的破坏力就被用于制造燃烧弹和烟雾弹,并应用到各种军事冲突中。
1943年7月28日的夜晚,德国汉堡火光冲天。英国出动787架轰炸机对汉堡进行轰炸,共投弹 2326吨,其中就包括大量含有白磷的燃烧弹。爆炸伴随着时速250公里的大风,引发了一场“火焰风暴”,熊熊大火烧了近3个小时。大量用于生产潜艇和武器的工厂、1万多座住宅、以及50多座历史悠久的教堂都被焚毁,约4.2万汉堡居民丧生。汉堡许多战后重建的房屋都标有“毁于1943年,重建于……”的字样。
磷诞生的圣米迦勒教堂侥幸躲过了这次轰炸,但一年后,还是在美军的空袭中严重损毁,直到1983年才被重新修建。汉堡作为磷的发现地,在二战中几乎被白磷燃烧弹夷为平地,这一可悲的历史巧合令人唏嘘。
除了二战时发生的几次大规模轰炸,在越南战争、海湾战争和叙利亚内战等多次军事冲突中,白磷弹都不时出现,造成大量人员伤亡。目前国际社会对于白磷弹的使用批评之声越来越多,但尚没有权威文件限制其使用。不知道这束死亡烟火还将持续多久。

美军在越南战争中使用白磷弹 图源:Wikipedia
致命毒物
磷不仅可以明火执仗地“杀人“,还可以悄无声息地“灭口”。
1935年,德国化学家施拉德 (Gerhard Schrader) 发现了一种速效有机磷杀虫剂——塔崩(Tabun)。塔崩是清澈无色的液体,还有着淡淡的水果香气,但仅仅吸入了很少量样品,施拉德和助手就成为了有机磷毒剂的首批受害者。他们出现了瞳孔收缩、呼吸困难及晕厥症状,三周后才逐渐康复。人们由此意识到塔崩的巨大毒性,并开启了有机磷神经毒剂这一潘多拉魔盒。
有机磷毒剂的致死原理是强烈抑制人体内的乙酰胆碱酶,从而使负责神经传递活动的乙酰胆碱不能被水解而蓄积,胆碱受体会因此而过度兴奋,最终导致中枢神经的麻痹瘫痪。
二战后,由于其巨大的军事潜力,研究人员开始深入地分析塔崩的化学结构,相继合成了一系列具有类似化学结构的新型神经性毒剂,沙林(Sarin)和VX是其中最具代表性的两种。
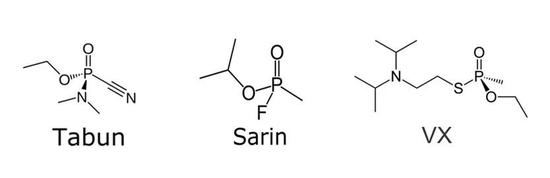
相比于人们所熟知的剧毒物质氰化钾,沙林的毒性还要再强烈20倍之多,大鼠的半数致死量只有26.2ppm。VX则是一种无色油状液体,比沙林更加危险,即使不通过吸入或注射的方式,只是接触皮肤也能迅速渗透到血液,5分钟内即可致人于死地。500mL的VX如果在空气中散布,足以杀死几万人,堪称化学武器中的核弹。
1995年东京地铁沙林毒气惨案,2018年某知名朝鲜男士在吉隆坡机场被袭身亡,直至最近发生的俄罗斯反对派人士中毒事件,都向全世界展示了有机磷神经毒剂的恐怖威力。
在介绍其他元素时,我们往往关注其价格之昂贵或用途之尖端,而磷在元素周期表中却无疑是一个独特的存在,一个诸多矛盾的集合体。
它的发现源自蒙昧时代炼金术师的痴心妄想,却强烈激发了欧洲人的好奇心和科学探索; 它参与造就了地球上的首个生命,却也是许多惨案背后的元凶;它遍布生命的每个细胞,却依然不能满足人类的巨大需求。
磷,关乎生死、善恶难辨。它可以造福人类,也可能毁灭家园。何去何从?这并不由磷,只取决于人。



